Không đảm bảo chất lượng thì dừng sản xuất": Trung Quốc siết chặt quản lý rủi ro trong gia công dược phẩm
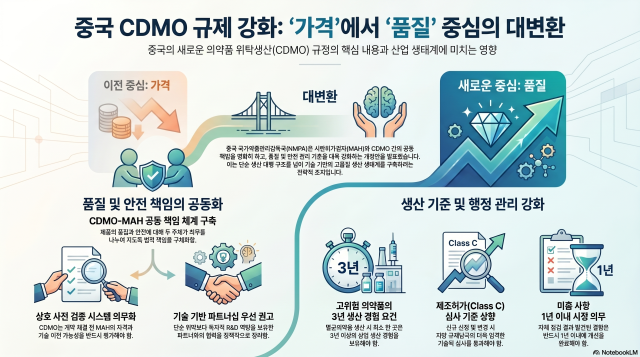
Chính phủ Trung Quốc đang đẩy mạnh cải cách lĩnh vực sản xuất dược phẩm theo hướng nâng cao chất lượng và siết chặt quản lý, thông qua việc sửa đổi các quy định liên quan đến sản xuất theo hợp đồng (CDMO). Động thái này được dự báo sẽ tác động đáng kể tới thị trường gia công dược phẩm toàn cầu.
Theo Trung tâm Nghiên cứu Kinh tế Sinh học thuộc Hiệp hội Công nghiệp Sinh học Hàn Quốc, ngày 14/4, National Medical Products Administration (NMPA) đã ban hành quy định sửa đổi về giám sát và quản lý sản xuất dược phẩm theo hợp đồng. Điểm đáng chú ý là việc chính thức hóa trách nhiệm chung giữa đơn vị sở hữu giấy phép lưu hành (MAH) và doanh nghiệp sản xuất gia công (CDMO) đối với chất lượng và an toàn sản phẩm.
Nâng vai trò CDMO: từ gia công sang chủ thể kiểm soát chất lượng
Theo quy định mới, CDMO không còn chỉ đóng vai trò sản xuất đơn thuần mà được nâng lên thành một chủ thể chịu trách nhiệm toàn diện trong chuỗi sản xuất. Các doanh nghiệp CDMO buộc phải xây dựng hệ thống đánh giá đối tác MAH, bao gồm năng lực quản lý chất lượng, mức độ rủi ro của sản phẩm và khả năng chuyển giao công nghệ. Chỉ những đối tác đạt yêu cầu mới được ký kết hợp đồng sản xuất.
Ngoài ra, NMPA khuyến khích CDMO ưu tiên hợp tác với các MAH có năng lực nghiên cứu – phát triển độc lập và sở hữu công nghệ cốt lõi, cho thấy định hướng chuyển từ mô hình gia công giá rẻ sang hợp tác dựa trên năng lực công nghệ.
Siết quy trình công nghệ và kiểm soát rủi ro
Quy định sửa đổi cũng đặt trọng tâm vào việc kiểm soát rủi ro trong quá trình chuyển giao công nghệ. MAH và CDMO phải đánh giá toàn diện các yếu tố liên quan như hệ thống phần mềm, thiết bị, quy trình và tiêu chuẩn chất lượng. Trong trường hợp phát hiện rủi ro khó kiểm soát, việc dừng dự án được khuyến nghị như một biện pháp đảm bảo an toàn.
Đối với các loại thuốc có rủi ro cao, đặc biệt là thuốc vô trùng, yêu cầu giám sát được nâng lên đáng kể. MAH phải thực hiện kiểm tra tại chỗ ít nhất mỗi năm một lần, đồng thời một trong hai bên (MAH hoặc CDMO) phải có tối thiểu 3 năm kinh nghiệm sản xuất thương mại đối với sản phẩm cùng loại.
Tăng cường kiểm soát hành chính và hậu kiểm
Về mặt quản lý nhà nước, các doanh nghiệp CDMO khi xin cấp mới hoặc điều chỉnh giấy phép sản xuất sẽ phải trải qua quy trình thẩm định nghiêm ngặt hơn từ cơ quan địa phương. Tất cả điều kiện theo quy định mới đều phải được đáp ứng đầy đủ trước khi được cấp phép.
Song song đó, NMPA yêu cầu các doanh nghiệp tiến hành tự kiểm tra theo tiêu chuẩn mới và hoàn thành việc khắc phục các thiếu sót trong vòng một năm. Trường hợp kéo dài hơn phải có giải trình cụ thể.
Tác động: “cú chuyển mình” về chất lượng, nhưng áp lực tăng cao
Giới chuyên gia nhận định, quy định mới sẽ thúc đẩy ngành CDMO Trung Quốc chuyển từ mô hình cạnh tranh chi phí sang cạnh tranh chất lượng và công nghệ, qua đó nâng cao uy tín trên thị trường quốc tế.
Tuy nhiên, trong ngắn hạn, các doanh nghiệp vừa và nhỏ có thể đối mặt với áp lực lớn do chi phí đầu tư cho hệ thống đánh giá, quản lý chất lượng và năng lực công nghệ tăng cao. Điều này có thể dẫn đến quá trình tái cấu trúc thị trường, trong đó các doanh nghiệp lớn hoặc có nền tảng công nghệ mạnh sẽ có cơ hội mở rộng thị phần.
Ý nghĩa rộng hơn: tái định vị trong chuỗi cung ứng toàn cầu
Việc Trung Quốc siết chặt quản lý CDMO không chỉ là điều chỉnh nội bộ mà còn phản ánh tham vọng nâng cấp vị thế trong chuỗi cung ứng dược phẩm toàn cầu. Khi tiêu chuẩn chất lượng được nâng lên, các doanh nghiệp Trung Quốc có thể cải thiện mức độ tin cậy với đối tác quốc tế.
Tuy vậy, liệu những thay đổi này sẽ giúp Trung Quốc vươn lên thành trung tâm sản xuất dược phẩm chất lượng cao hay làm chậm lại tốc độ tăng trưởng do gánh nặng chi phí vẫn là câu hỏi phụ thuộc vào khả năng thích ứng của doanh nghiệp trong thời gian tới.
© Bản quyền thuộc về Thời báo Kinh tế AJU & www.ajunews.com: Việc sử dụng các nội dung đăng tải trên vietnam. kyungjeilbo.com phải có sự đồng ý bằng văn bản của Aju News Corporation.






