[Kinh tế Nhật báo] Các công ty sinh học Hàn Quốc đang đẩy nhanh mở rộng thị trường toàn cầu bằng cách tận dụng quy trình phê duyệt nhanh của Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) trong lĩnh vực điều trị ung thư đường mật.
ABL Bio và HLB đang dẫn đầu với các ứng viên thuốc mới có cơ chế khác biệt, có khả năng thay đổi cục diện thị trường điều trị ung thư đường mật thứ cấp, nơi nhu cầu chưa được đáp ứng cao.
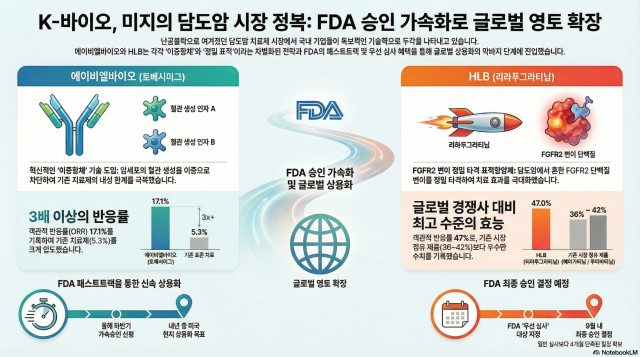
Theo ngành công nghiệp, Toveshimig (ABL001) của ABL Bio, đã được xuất khẩu công nghệ cho Compass Therapeutics tại Mỹ, đã hoàn thành thử nghiệm lâm sàng giai đoạn 2/3 toàn cầu và chuẩn bị công bố dữ liệu. Toveshimig sử dụng công nghệ 'kháng thể kép' để ngăn chặn sự hình thành mạch máu, vượt qua hạn chế của các liệu pháp kháng thể đơn lẻ trước đây. Tỷ lệ phản ứng khách quan (ORR) đạt 17,1%, gấp ba lần so với tiêu chuẩn hiện tại là 5,3%.
Đã được FDA chỉ định là đối tượng 'xem xét nhanh', Toveshimig dự kiến công bố dữ liệu trung gian vào tháng 4. Nếu dữ liệu này có ý nghĩa thống kê, ABL Bio sẽ nộp đơn xin phê duyệt nhanh trong nửa cuối năm nay, mở ra khả năng thương mại hóa tại Mỹ vào năm sau.
HLB cũng không kém cạnh. Thông qua công ty con Elevate tại Mỹ, HLB đã bắt đầu quy trình xem xét đơn xin cấp phép thuốc mới (NDA) cho Lirafugratinib (RLY-4008). Đặc biệt, Lirafugratinib đã được FDA chỉ định là đối tượng 'xem xét ưu tiên', rút ngắn thời gian xem xét xuống còn 6 tháng, với quyết định cuối cùng dự kiến trước ngày 27 tháng 9. Lirafugratinib nhắm mục tiêu chính xác vào biến thể protein FGFR2, đạt ORR 47% trong thử nghiệm, vượt trội so với Pemigatinib (36%) và Futibatinib (42%).
Ngành công nghiệp phân tích rằng HLB đang xây dựng một danh mục mạnh mẽ trong thị trường thuốc chống ung thư toàn cầu, cùng với thuốc điều trị ung thư gan Rivoceranib đang chờ phê duyệt của FDA.
Các công ty sinh học Hàn Quốc tập trung vào thị trường ung thư đường mật Mỹ vì đây là loại ung thư 'âm thầm', khó phát hiện sớm và thường được chẩn đoán khi không thể phẫu thuật. Tỷ lệ tái phát sau phẫu thuật cũng rất cao, và thiếu các liệu pháp điều trị thứ cấp sau thất bại điều trị đầu tiên. Do đó, FDA áp dụng các chính sách linh hoạt như phê duyệt nhanh, xem xét ưu tiên và chỉ định thuốc mồ côi cho các liệu pháp điều trị ung thư đường mật.
Một chuyên gia trong ngành cho biết: "Trước đây, sinh học Hàn Quốc bị chỉ trích là 'hy vọng hão', nhưng giờ đây đã chứng minh năng lực thông qua dữ liệu khách quan và quy trình chính thức của FDA. Đặc biệt, nếu các công ty của chúng ta có thể trở thành người tiên phong hoặc tốt nhất trong lĩnh vực không có giải pháp thay thế như ung thư đường mật, thì đây sẽ là cơ hội để củng cố ảnh hưởng toàn cầu của K-bio."
* Bài viết này được dịch tự động bằng AI.
© Bản quyền thuộc về Thời báo Kinh tế AJU & www.ajunews.com: Việc sử dụng các nội dung đăng tải trên vietnam. kyungjeilbo.com phải có sự đồng ý bằng văn bản của Aju News Corporation.



