[Kinh tế Nhật báo] GC Green Cross đã quyết định ngừng phát triển thuốc điều trị bệnh máu khó đông thế hệ mới và chọn chiến lược 'lựa chọn và tập trung'. Sự xuất hiện của thuốc mới từ Pfizer với cùng cơ chế đã khiến GC Green Cross quyết định chuyển hướng sang các loại thuốc điều trị bệnh hiếm khác có tiềm năng thành công cao hơn.
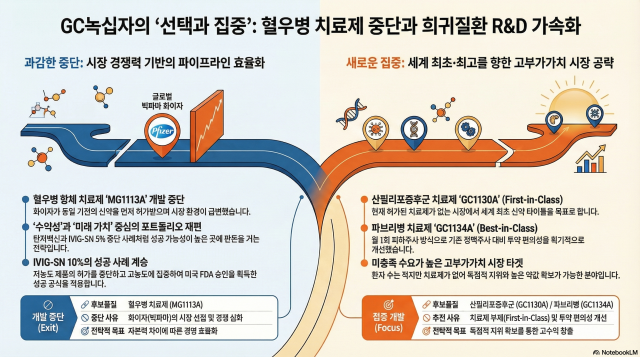
Ngày 24 tháng 3, theo ngành công nghiệp, GC Green Cross đã xác nhận ngừng phát triển thuốc điều trị bệnh máu khó đông loại A và B 'MG1113A' ở giai đoạn thử nghiệm lâm sàng 1b. Đây được coi là một chiến lược tối ưu hóa đường ống điển hình, tập trung nguồn lực vào các dự án có khả năng thành công cao hơn.
Bệnh máu khó đông là một bệnh di truyền do thiếu yếu tố đông máu, khiến máu không đông lại được. Trước đây, bệnh nhân phải chịu đựng việc tiêm tĩnh mạch 2-4 lần mỗi tuần để bổ sung yếu tố đông máu. 'MG1113A' của GC Green Cross được kỳ vọng là 'người thay đổi cuộc chơi' khi chỉ cần tiêm dưới da một lần mỗi tuần.
Tuy nhiên, thị trường đã thay đổi nhanh chóng khi Pfizer đã được cấp phép cho thuốc 'Hemlibra' với cùng cơ chế 'ức chế TFPI', chiếm lĩnh thị trường nội địa.
GC Green Cross không phải lần đầu tiên thực hiện quyết định 'ngừng táo bạo' như vậy. Trước đây, họ đã ngừng phát triển vắc xin bệnh than 'GC1109' và sản phẩm 'IVIG-SN 5%' tại Mỹ để tập trung vào các sản phẩm có tiềm năng cao hơn.
Hiện tại, GC Green Cross đang tập trung phát triển thuốc điều trị 'hội chứng Sanfilippo (MPS IIIA)' và 'bệnh Fabry'. Đây là những thị trường có giá trị cao do thiếu thuốc điều trị và giá thuốc rất đắt.
Đặc biệt, thuốc điều trị hội chứng Sanfilippo A 'GC1130A' đang được kỳ vọng sẽ trở thành 'thuốc mới đầu tiên trên thế giới'. Hiện tại, GC Green Cross đang tiến hành thử nghiệm lâm sàng giai đoạn 1 tại Hàn Quốc và Mỹ.
Thuốc điều trị bệnh Fabry 'GC1134A' cũng là một ứng viên tiềm năng, với khả năng tiêm dưới da một lần mỗi tháng. Sản phẩm đã được FDA và cơ quan y tế Hàn Quốc công nhận là thuốc mồ côi, mang lại nhiều lợi ích về thuế và quyền bán độc quyền.
Một chuyên gia trong ngành cho biết, “Sự khác biệt về vốn giữa các công ty dược phẩm trong nước và các công ty lớn toàn cầu là rất lớn, do đó việc sớm loại bỏ các ứng viên không cạnh tranh là một phần của quá trình tối ưu hóa quản lý.”
* Bài viết này được dịch tự động bằng AI.
© Bản quyền thuộc về Thời báo Kinh tế AJU & www.ajunews.com: Việc sử dụng các nội dung đăng tải trên vietnam. kyungjeilbo.com phải có sự đồng ý bằng văn bản của Aju News Corporation.



